Chlamydie
Chlamydie to Gram-ujemne bakterie wewnątrzkomórkowe. Mikroorganizmy te po wtargnięciu do organizmu przyczepiają się do komórek gospodarza, następnie wnikają do nich i podobnie jak wirusy mnożą się wewnątrz komórek, a następnie rozprzestrzeniają po całym organizmie drogą krwionośną, przewlekle infekując układ naczyniowy i nie tylko.
Istnieją trzy gatunki chlamydii patogennych dla ludzi:
1. C. pneumoniae – przenoszona drogą kropelkową;
2. C. trachomatis – przenoszona drogą płciową;
3. C. psittaci – przenoszona przez kontakt z chorym ptactwem;
Chlamydia trachomatis przenoszona jest przede wszystkim droga płciową, dlatego też najczęściej powoduje problemy i choroby związane z układem moczowo-płciowym. Infekcja może przebiegać bzobjawowo, jednak najczęściej pojawiają się objawy typu pieczenie oraz ból cewki moczowej, dyskomfort podczas oddawania moczu, rożnego rodzaju wydzieliny wydostające się z cewki moczowej. U mężczyzn dodatkowymi objawami mogą być bóle w okolicy podbrzusza oraz nadwrażliwość lub ból jąder. Może powodować przerost gruczołu prostaty spowodowany stanem zapalnym, a także prowadzić do niepłodności.
Zakażenie C. trachomatis jest szczególnie groźne dla kobiet. co w konsekwencji może prowadzić do bezpłodności lub powikłań ciąży. Dyskomfort przy oddawaniu moczu zaczerwienienia, opuchlizny to najczęstsze objawy zapalenia szyjki macicy. Często ma ono charakter bez objawowy. Przy stanach przewlekłego zakażenia bakteria ta może powodować zmiany nowotworowe szyjki macicy. Poprzez jej obecność w drogach rodnych staje się kofaktorem wirusa brodawczaka ludzkiego typ 16. Chlamydia trachomatis często jest również przyczyną zapalenia moczowodów z równoczesnym ropomoczem oraz stanem zapalnym narządów miednicy mniejszej. Infekcja może spowodować przerost błon śluzowych macicy, zapalenie jajowodów, a nawet ropień jajników, w konsekwencji czego może doprowadzić do bezpłodności. Jest również niebezpieczna dla noworodków. Zakażenie może powstać podczas porodu, powodując szereg dolegliwości ze strony układu oddechowego oraz zmysłu wzroku. U noworodków często C. trachomatis może być przyczyną zapalenia płuc. Dotyczy ono dzieci między 2 a 16 tygodniem życia, przebiega zazwyczaj bezgorączkowo, z przyspieszonym oddechem i pracą serca, lekkim napadowym kaszlem. Niezdiagnozowane lub nieleczone chlamydialne zapalenie płuc może doprowadzić do trwałego uszkodzenia układu oddechowego. Badania potwierdzają, że Chlamydia trachomatis ma swój udział w etiologii nagłej śmierci niemowląt (SIDS).
C. trachomatis może zainfekować również narządy wewnętrzne. Narządy moczowo-płciowe dzieli nie wielka droga do wątroby, śledziony trzustki, nerek czy wyrostka robaczkowego, dlatego też mogą one zostać zaatakowane.
Chlamydia pneumoniae budową przypomina bakterię Gram(-). Ma trójwarstwową błonę zewnętrzną i podobnie jak inne gatunki Chlamydii wystepuje w dwóch odrębnych formach – jako pozakomórkowe, nieaktywne metabolicznie, lecz zakaźne ciało elementarne (EB), o kształcie owalnym lub gruszkowatym oraz większe ciało siateczkowate.
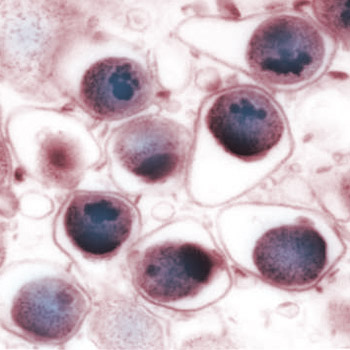
Chlamydia pneumoniae wystepuje powszechnie na całym świecie. Zakażenia szerzą się drogą powietrzno-kropelkową, zwłaszcza w środowiskach zamkniętych, z człowieka na człowieka. Mają one najczęściej przebieg bezobjawowy lub łagodny i w większości przypadków nie są diagnozowane i rozpoznawane. Pierwotne zakażenie C. pneumoniae pojawia się na ogół w dzieciństwie, najczęściej między 5 a 10 rokiem życia. Rocznie ulega zakażeniu około 6-9% dzieci w wieku szkolnym. W późniejszym okresie życia następują zazwyczaj reinfekcje. Określa się je wspólną nazwą nawracających zakażeń. Szacuje się, że w ciągu życia każdy dwu- lub trzykrotnie może przechodzić zakażenie Chlamydię pneumoniae. Przeglądy seroepidemilogiczne wykazały, że 50-70% osób dorosłych ma swoiste przeciwciała, a ich częstość wzrasta z wiekiem. Badania wykazały, że przeciwciała występują częściej u mężczyzn niż u kobiet. Zarówno u dorosłych jak i u dzieci zakażenie może mieć przebieg ostry (szczególnie gdy współtowarzyszy innemu zakażeniu, spowodowanemu np. przez Streptococcus pneumoniae) lub przewlekły. Może przebiegać także bezobjawowo lub ze skąpymi objawami klinicznymi i wtedy bywa często nie rozpoznawane.
Zakażenia układu oddechowego
Chlamydia pneumoniae wywołuje zakażenia górnych i dolnych dróg oddechowych. Może powodować zapalenie gardła, krtani, ucha środkowego i zatok, zapalenie oskrzeli oraz tzw. atypowe zapalenie płuc. U około 9% pacjentów stwierdza się obecność C. pneumoniae w aspiracie ucha i w 5% materiałów pobranych z zatok. Zakażenie ucha środkowego i zatok może przebiegać jako izolowana jednostka chorobowa lub może towarzyszyć objawom ze strony układu oddechowego.
Częstość pozaszpitalnych zapaleń płuc o etiologii chlamydiowej oceniana jest na około 5-15%, a w okresach epidemicznych nawet do 40%. Chorują najczęściej dzieci i młodzi dorośli. U pacjentów hospitalizowanych pnaumonie chlamydiowe występują w podobnym odsetku (6-10%), ale zazwyczaj dotyczą osób starszych (>60 r.ż.) i związane są z istniejącym chronicznym zakażeniem. Chlamydiowe zapalenia płuc u osób młodych na przebieg dość łagodny, manifestuje się klinicznie tylko u około 10% zakażonych. Ciężki przebieg, występuje w przypadkach konfekcji. Choroba charakteryzuje się dwufazowością. Objawy ze strony górnych dróg oddechowych, najczęściej zapalenie gardła i chrypka, poprzedzają na 1-4 tygodni zapalanie płuc. Najczęstszymi jego objawami jest gorączka i kaszel. Plwocina nie ma charakteru ropnego, u niektórych pacjentów w ogóle nie występuje. Odczyn Biernackiego jest miernie podwyższony, liczba leukocytów we krwi obwodowej jest prawidłowa. Zmiany cofają się szybciej niż w zapalenia płuc wywołanym przez większość innych drobnoustrojów.
Patomechanizm zakażeń wywołanych przez C. pneumoniae podobnie jak w przypadku innych drobnoustrojów wewnątrzkomórkowych, uwarunkowany jest oddziaływaniem układu immunologicznego gospodarza ze specyficznymi antygenami eksponowanymi na powierzchni komórki. W rozwoju zapalenia płuc uczestniczą makrofagi pęcherzyków płucnych, komórki mięśniowe i śródbłonka, w których chlamydie mogą się namnażać. Bakterie mogą być następnie przenoszone na obwód drogą krwi przez monocyty/makrofagi, stąd powikłaniem zapalenia płuc może być zapalenie stawów i rumień guzowaty, zajęte mogą być też mięsień sercowy, wątroba i nerki.
Zakażenie Chlamydią pneumoniae a astma oskrzelowa
W ostatnich latach coraz więcej uwagi zwraca się na rolę C. pneumoniae w rozwoju astmy oskrzelowej oraz przewlekłej obturacyjnej choroby płuc. Wiadomo bowiem, że zakażenia dróg oddechowych, zarówno wirusowe jak i bakteryjne mają wpływ na wytworzenie się nieswoistej nadreaktywności drzewa oskrzelowego i zapoczątkowanie astmy infekcyjnej. Wieloośrodkowe badania przeprowadzone w grupie ponad 4000 pacjentów pozwoliły ustalić przyczynową rolę C. pneumoniae w epizodach zaostrzeń astmy oskrzelowej u 5-23% pacjentów. Wykazano ponadto, że objawy spastycznego zapalenia oskrzeli występują częściej u dorosłych niż u dzieci i SA zazwyczaj wynikiem reinfekcji lub zakażenia przewlekłego C. pneumoniae, a nie infekcji pierwotnej. Doniesienia literaturowe próbują także udowodnić udział C. pneumoniae w rozwoju sarkoidozy i pierwotnych nowotworów płuc.
Udział Chlamydia pneumoniae w chorobach układu krążenia
Chlamydia pneumoniae może odgrywać rolę przyczynową w wielu stadiach rozwoju miażdżycy – choroby rozwijającej się przez niemal całe życie, a przez to również w rozwoju choroby wieńcowej serca. C. pneumoniae może brać udział w zapoczątkowaniu choroby, jak też w różnych etapach jej rozwoju; może również przyspieszać jej rozwój. Badania potwierdzają udział C. pneumoniae w rozwoju i przyspieszaniu progresji choroby, nie wykluczają również udziału tego patogenu w jej zapoczątkowaniu. C. pneumoniae może również uczestniczyć w końcowych etapach choroby, kiedy powikłania miażdżycy doprowadzają do zawału serca lub udaru mózgu. Wykazano częste występowanie przeciwciała antychlamydiowych u osób z chorobą nadciśnieniową, tętniakami aorty brzusznej, zawałem mózgu i chorobą zakrzepową.
Doniesienia dotyczące związku choroby wieńcowej z czynnikami infekcyjnymi pojawiły się już w latach 70. Związek zakażenia C. pneumoniae z chorobami układu krążenia opisano w wielu krajach, na podstawie badań seroepidemiologicznych, anatomopatologicznych i prac doświadczalnych. Zespół prof. P. Saikku w 1988 roku jako pierwszy opisał związek między obecnością swoistych przeciwciał anty-C. pneumoniae a chorobą wieńcową serca. Ten sam zespół wykrył obecność kompleksów immunologicznych, zawierających lipopolisacharyd (LPS) C. pneumoniae u ponad 60% chorych z ostrym zawałem serca. Kolejne badania prospektywne pokazały, że przewlekłe zakażenie C. pneumoniae może stanowić niezależny czynnik ryzyka w rozwoju choroby niedokrwiennej i miażdżycy naczyń. Alan Shor przy użyciu mikroskopu elektronowego wykrył w blaszce miażdżycowej obecność struktur, przypominających swym gruszkowatym kształtem C. pneumonie. C.-C. Kuo metodą immunohistochemiczną z użyciem przeciwciał monoklonalnych oraz Ann Lee Campbell metodą PCR wykazali, że struktury obserwowane przez Shora to istotnie C. pneumoniae. Udało się również wyhodować ten drobnoustrój ze skrawków tętnic; wykazano w ten sposób, że C. pneumoniae żyje i może namnażać się w tkance naczyń. C. pneumoniae jako jedyny gatunek z rodzaju Chlamydia może namnażać się we wszystkich niemalże typach komórek, znajdujących się w blaszce miażdżycowej – w makrofagach, komórkach mięśni gładkich i komórkach śródbłonka. Co ciekawe, nie stwierdzono obecności tego drobnoustroju w otaczającej zmianę miażdżycową zdrowej tkance. Zakażenie komórek śródbłonka wzmaga ekspresję ich molekuł powierzchniowych, co ułatwia migrację neutrofili i makrofagów oraz ich adhezję i wywołuje odczyn zapalny. Wywołuje ono również sekrecję czynnika III (tromboplastyny tkankowej), co sugeruje, że C. pneumoniae może modulować aktywność procesów krzepnięcia. Zakażenie makrofagów przez C. pneumoniae powoduje wydzielanie cytokin, które przyczyniają się do podtrzymywania stanu zapalnego i progresji zmian miażdżycowych. Ponadto, zakażenie makrofagów przez C. pneumoniae lub stymulowanie ich chlamydiowym LPS-em, zapoczątkowuje przekształcanie się ich w komórki piankowate, które są charakterystyczne dla wczesnych zmian miażdżycowych. Powyższe dane wskazują, że zakażenie C. pneumoniae wywołuje szereg zmian zapalnych, charakterystycznych dla wczesnych i zaawansowanych zmian miażdżycowych.
Badania in vitro prowadzone na ludzkich makrofagach wykazały, że po dodaniu do podłoża cholesterolu LDL, makrofagi fagocytują go. Jeśli jednak makrofagi zakażono C. pneumoniae, fagocytowały one znacznie większe ilości LDL-u, a wiele z nich przekształcało się w komórki piankowate.
Innym postulowanym mechanizmem, przez który infekcja Chlamydia pneumoniae może wpływać na naczynia tętnicze w chorobie nadciśnieniowej, jest wywoływanie reakcji autoimmunologicznej przez stymulację produkcji immunoglobulin skierowanych przeciw białkom szoku cieplnego. Wykazano, że chlamydiowe białka szoku termicznego (hsp-60) są obecne w blaszce miażdżycowej i mogą uczestniczyć w najistotniejszych mechanizmach rozwoju miażdżycy i jej następstw. Białka szoku cieplnego (HSP, heat Srock protein) stanowią rodzinę białek o bardzo homologicznej sekwencji aminokwasów, ich struktura niewiele się różni między gatunkami. Dlatego też przeciwciała i limfocyty T skierowane przeciw HSP65/ /HSP60 bakterii Chlamydia pneumoniae mogą reagować krzyżowo z HSP60 człowieka. Rozpowszechnienie infekcji tymi patogenami wśród chorych na nadciśnienie jest więc podobne do częstości klasycznych czynników ryzyka w tej grupie chorych: zaburzeń lipidowych, palenia tytoniu czy nadwagi/otyłości.
Objawy ze strony układu ruchu
Przy przewlekłym zakażeniu bakterią Chlamydii płucnej może również dochodzić do chorób układu ruchu. Przede wszystkim są tutaj narażone stawy. Bakteria może powodować zapalenie stawów, wszelkiego rodzaju bóle oraz zwyrodnienia.
Wpływ na układ nerwowy
Dzięki przeprowadzonym badaniom na obecność DNA Chlamydii pneumoniae w komórkach układu nerwowego oraz osłonkach mielinowych dowiedziono, że może mieć ona związek z wieloma chorobami układu nerwowego. Chorzy cierpiący na stwardnienie rozsiane (SM), które polega na rozpadzie osłonek mielinowych substancji białej mózgu spowodowane może być przez Chlamydię. Badania wykazały również, że bakteria ta może mieć wpływ na inne schorzenia neurologiczne. Jedną z takich chorób jest Alzheimer.
Chlamydia psittaci
Człowiek narażony na zakażenie tą bakterią może zachorować na papuzicę, zwaną inaczej ptasią chorobą. Rezerwuarem bakterii są ptaki. Do zakażenia może dochodzić drogą oddechową, lub bezpośredni kontakt z zarażonym zwierzęciem. Przebieg choroby często jest bezobjawowy, natomiast objawy jakie mogą wystąpić to atopowe zapalenie płuc, gorączka. Wymienione objawy często łączone są z typową infekcją grypopodobną. W bardzo rzadkich przypadkach dochodzi do stanu zapalnego mięśnia sercowego, opon mózgowych czy rdzenia kręgowego.

